Scientific journal
Scientific Review. Chemical sciences
DEVELOPMENT OF A RAPID METHOD FOR QUANTIFYING THE SUM OF SANGUINARINE AND CHELERYTHRINE (BISULFATES) CALCULATED AS SANGUIRITRIN IN MACLEAYA HERBA BY SPECTROPHOTOMETRY
Маклейя сердцевидная (Macleaya cordata (Willd.) R. Br.), маклейя мелкоплодная (Macleaya microcarpa (Maxim.) Fedde) сем. Papaveraceae и их гибрид маклейя кьюская (Macleаya х kevensis Turill) – многолетние травянистые растения родом из Восточной Азии, широко используется в качестве лекарственного растительного сырья (ЛРС) в Китае, России, США и др. странах [1, 2].
ЛРС маклейи являются важным источником биологически активных соединений (БАВ) – изохинолиновых алкалоидов, которых содержится в маклейе более 140 соединений, относящимся к группам бензофенантридина, протоберберина, протопина и др. (сангвинарин, хелеритрин, протопин, берберин, 6-гидроксиметил-7,8-демилендигидрохелеритрин, 6-гидроксиметилдигидросангинарин, нандазурин, гидроксихелидонин, капауридин, (-)-дицентрин, лептопин, адлумидин, такатонин, (2,3)-транс-N-(п-гидроксифенетил)феруламид, 9-этоксиаристололактам, таликминин, касситидин, ацетилизокоринолин, оксинитидин, криназиатин, зантоксилин и 7,9-диметокси-2,3-метилендиоксибензофенантридин, 2,3-метилендиокси-7,10-диметил-7,8,9,10-тетрагидробензохинолин, 2,3-метилендиокси-7,10-диметил-8-карбоксилбензохинолин и др.) [3-5]. Из надземной части маклейи были выделены энантиомерные димеры алкалоидов, (±)-маклеаинов А (1) и В (2), представляющих собой продукт димеризации двух разных типов алкалоидов через σ-связь C–C. [6]
Также в ЛРС содержатся фенилпропаноиды, флавоноиды, терпеноиды, стероиды, органические кислоты и др. [2, 7, 8].
Важность исследуемого ЛРС подтверждает объем мирового рынка экстрактов маклейи, который в 2022 году составил 34 млн долл. США, а к 2031 году, по прогнозам, он достигнет 113,78 млн долл. США, что соответствует среднегодовому темпу роста в 14,4% в течение указанного периода [9].
В России ЛРС маклейи используется используются для получения лекарственного препарата противовоспалительного и противомикробного действия «Санвиритрин», действующими веществами которого являются сумма хелеритрина и сангвинарина бисульфатов, [6], за рубежом представлены экстракты «Macleaya cordata extract» CAS 112025-60-2 (смесь хелеритрина и сангвинарина хлоридов с содержанием 35%, 60%, 80%), «Sangrovit» (содержание суммы четырех алкалоидов сангвинарина, хелеритрина, протопина и аллокриптопина - 1,25%, из них 0,5% сангвинарина), «Sanguirisal» (смесь хелеритрина и сангвинарина салицилатов) и др. [10, 11].
Экстракты маклейи, содержащие хелеритрин и сангвинарин, обладают широким спектром фармакологического действия – противовоспалительным, противомикробным, антиоксидантным, проапоптотическим, противоопухолевым, инсектицидным, фунгицидным [12-15].
Выделенные из маклейи сердцевидной алкалоиды протопинового типа на модели воспаления кишечника у мышей, вызванного липополисахаридами, обуславливают различные терапевтические эффекты, приводящие к улучшению морфологии кишечника, увеличению содержания бокаловидных клеток кишечника, снижению уровня провоспалительных цитокинов, восстановлению микрофлоры [16].
Экстракты и алкалоиды маклейи перспективны для применения не только в качестве лекарственных средств, но и в качестве кормовых добавок в аквакультуре, зоотехнологии, птицеводстве и др. [10, 16-21]. Экстракт маклейи сердцевидной - потенциальный антибиотик, его прием улучшает состояние эпителия желудочно-кишечного тракта и гуморальную реакцию у коз [22]; улучшает состояние кишечника, микробиоту кур-несушек и качество яиц [23]. Выявлено защитное действие изохинолиновых алкалоидов маклейи сердцевидной на липополисахарид-индуцированное повреждение печени у птиц [24].
Преимуществом экстракта маклейи является отсутствие токсичности, генотоксичности, мутагенности и тератогенности [25]. Выявлена стабильность сангвинарина и хелеритрина из маклейи сердцевидной в метаноле и этаноле, в воде при температуре ниже 54 °C; сангвинарин стабилен при pH 2,5 - 7,0, а хелеритрин - при pH 2,5 - 8,0; оба алкалоида нестабильны в водопроводной воде и при взаимодействии с окислителями [26].
Для качественного и количественного анализа алкалоидов маклейи используют хроматографические методы, например, метод изократической ВЭЖХ в сочетании с электрораспылительной масс-спектрометрией, высокоскоростной противоточной хроматографии, модифицированной ионной жидкостью, обращенно-фазовой ВЭЖХ с тандемной масс-спектрометрией, ВЭЖХ с тандемной квадруполь-времяпролётной масс-спектрометрией и др. [3, 4, 15, 18, 27, 28] .
Для оценки содержания суммы алкалоидов успешно применяется спектрофотометрические методы. Определение суммы бензо[с]фенантридиновых алкалоидов в пересчете на сангвиритрин проводят в метанольных и этанольных извлечениях при аналитической длине волны 452 нм [29-31] и 332±3 нм [32].
В настоящее время содержание суммы сангвинарина и хелеритрина в траве маклейи регламентируется требованиями ФС.2.5.0119 «Маклейи трава» - не менее 0,5 % суммы алкалоидов в пересчёте на сангвинарин + хелеритрин в сухом сырье; определение проводят после подщелачивания и экстракции оснований алкалоидов из измельченного сырья хлороформом в течение 15 ч. Количественное определение проводят с использованием 5% раствора уксусной кислоты.
В предыдущей версии ФС 42-2666-89 наряду с экстракцией хлороформом использовали ТСХ для отделения алкалоидов от сопутствующих веществ, в качестве растворителя - подкисленный метиловый спирт. Оптическую плотность растворов измеряли на спектрофотометре в изобестической точке при длине волны 452 нм.
По методике определения с экстракцией хлороформом без реэкстракции результаты будут существенно завышенными, из-за вклада пигментов в поглощение в видимой области спектра. По экспериментальной оценке вклада пигментов в оптическую плотность, таковая может увеличивать на 20-30% от собственно суммы алкалоидов.
Хлороформ с водой при рН больше 7 создает стойкие эмульсии, что значительно уменьшает точность определения и увеличивает его время из-за сложности разделения фаз, требующей использования дополнительного оборудования (центрифуги).
На извлечение алкалоидов оказывает влияние температура, при настаивании с хлороформом при комнатной температуре в течение 30 мин нельзя достичь исчерпывающей экстракции, это обстоятельство также очень сильно влияет на погрешность определения.
Использование в качестве аналитической длины волны 402 нм – дает завышенные результаты из-за соизвлекаемых вместе с алкалоидами веществ, поглощающих в этой области спектра. Пересчет содержания суммы алкалоидов на неопределенную сумму двух веществ «сангвинарин + хелеритрин» недостаточно корректный, необходимо использовать только один конкретный стандартный образец вещества или же стандартизированную субстанцию.
В процесс извлечения алкалоидов из ЛРС маклейи решающим этапом в подготовке раствора для качественного и количественного определения является их полная экстракция и максимальное отделение от других сопутствующих веществ. Поскольку большинство изохинолиновых алкалоидов и их солей является липофильными соединениями, то экстракцию можно успешно проводить спиртами (метанол, этанол, бутанол, октанол и т.д.), как длительным настаиванием при комнатной температуре, так и экстракцией при нагревании и при перемешивании [14, 26, 33-36].
Бензофенантридиновые алкалоиды из ЛРС хорошо извлекаются этанолом [11, 15, 18]. В качестве экстрагентов широко используют подкисленную воду и растворы кислот (хлористоводородной, серной, фосфорной, уксусной, муравьиной и др.) [3, 37, 38]. Алкалоиды маклейи сердцевидной успешно экстрагировали хлористоводородной кислотой 0,2 моль/л, затем алкалоидные соединения извлекали из деминерализованного экстракта органическими растворителями, после чего анализировали методом УВЭЖХ-ДМД-МС/МС [3].
Особенностью использования в качестве экстрагентов растворов кислот является то, что они наряду с алкалоидами извлекают все остальные водорастворимые соединения, но не соизвлекают липофильные соединения. Преимущество этанола в качестве экстрагента состоит в использовании нетоксичного растворителя, возможности извлекать алкалоиды как в виде солей, так и оснований, при этом полисахариды и белковые соединения не извлекаются, недостатком является извлечение большого количества примесей. Для полноты извлечения органическими растворителями, например хлороформом, и их смесями используют подщелачивание, что позволяет проводить исчерпывающую экстракцию алкалоидов в виде оснований. Следует отметить, что существенным недостатком использования хлороформа, метиленхлорида и диэтилового эфира является их способность образовывать со спирто-водными растворами стойкие эмульсии, что затрудняет определение, увеличивает его время и привносит значительную погрешность в результаты. Также хлорсодержащие экстрагенты являются токсичными и экологически опасными растворителями, характеризуются извлечением большого количества других веществ, содержащихся в растении – фенольных соединений, пигментов, углеводородов и пр. Поэтому для отделения суммы алкалоидов от сопутствующих веществ целесообразно использовать последовательные стадии экстракции - реэкстракции водно-спиртовыми, водно-кислотными растворами и органическими экстрагентами с добавлением щелочи [39, 40].
Целью работы являлась разработка методики определения количественного определения суммы сангвинарина и хелеритрина в пересчете на сангвиритрин в траве маклейи методом спектрофотометрии, а также сравнение содержания суммы алкалоидов в образцах травы разных видов сырья - маклейи сердцевидной и мелкоплодной.
Материалы и методы. Объектом исследования служили образцы травы M. cordata и M. microcarpa, выращенные на опытных полях Средне-Волжского филиала ФГБНУ ВИЛАР в 2022-23 г. и поступившие на анализ в Испытательный центр ФГБНУ ВИЛАР.
Спектры поглощения в видимой и УФ-области получали на двулучевых спектрофотометрах Cary 100 Scan (Varian, США) и Shimadzu UV-1800 (Япония); для взвешивания использовали весы аналитические Vibra Shinko Denshi, класс 2 HRT-220CE; для получения растворов мерную посуда 1-го класса точности.
Испытуемый раствор: лекарственное растительное сырье (ЛРС) меклейи измельчают до размера частиц, проходящих сквозь сито с отверстиями размером 1 мм. Около 1,0 г (точная навеска) ЛРС помещают в коническую колбу со шлифом, прибавляют 50 мл спирта 70%, взвешивают и нагревают на кипящей водяной бане в течение 1 ч. Затем колбу отсоединяют от холодильника, охлаждают до комнатной температуры, доводят до первоначального веса спиртом 70% и фильтруют через бумажный складчатый фильтр. 5 мл полученного извлечения помещают в делительную воронку, прибавляют 2 мл 10% аммиака, 10 мл этилацетата, 5 мл воды очищенной и осторожно взбалтывают в течение 1 мин. После расслоения фаз (слои должны быть прозрачны) верхний (этилацетатный) слой отделяют в химический стакан вместимостью 50 мл. Экстракцию проводят еще раз с 5 мл этилацетата, после расслоения прозрачный этилацетатный слой отделяют и помещают в тот же стакан.
Объединенные этилацетатные извлечения из стакана количественно переносят в делительную воронку, в стакан прибавляют 10 мл воды, ополаскивают и переносят в ту же делительную воронку, осторожно взбалтывают в течение 1 мин (промывают от аммиака и сопутствующих окрашенных водорастворимых веществ). После расслоения фаз, когда нижняя (водная) фаза станет прозрачной, ее сливают и отбрасывают. К этилацетатному извлечению в делительную воронку прибавляют 2 мл кислоты серной 16%, 10 мл воды очищенной и аккуратно взбалтывают в течение 2 мин (водный слой окрашивается в желтый цвет). После разделения фаз (верхняя фаза должна быть прозрачной) водное извлечение отделяют, а с этилацетатным извлечением проводят еще двукратную экстракцию с 5 мл воды каждый раз, затем этилацетатную фазу отбрасывают, а объединенную водную фазу помещают в делительную воронку, прибавляют 5 мл аммиака 25%, 10 мл этилацетата и взбалтывают в течение 1 мин. Слои должны стать бесцветными. Этилацетатное извлечение после расслоения фаз (нижняя, водная, фаза должны быть прозрачной) отделяют в круглодонную колбу вместимостью 50-100 мл, экстракцию проводят еще два раза по 5 мл этилацетата каждый раз, этилацетатные слои отделяют и помещают в ту же колбу.
Растворитель из объединенного этилацетатного извлечения отгоняют на вакуум-выпарном аппарате при температуре около 60°С до объема около 0,05 мл, в колбу к остатку прибавляют 8 мл спирта 70%, подкисленного серной кислотой, выдерживают около 2 мин при периодическом взбалтывании, затем сливают в мерную колбу вместимостью 10 мл. В круглодонную колбу прибавляют еще 2 мл спирта 70%, подкисленного серной кислотой, взбалтывают, жидкость сливают в ту же мерную колбу, доводят спиртом 70%, подкисленным серной кислотой, до метки и перемешивают.
Раствор стандартного образца (СО) сангвиритрина
Раствор СО сангвиритрина. Около 0,01 г (точная навеска) сангвиритрина (ФС 42-0198-07) помещают в мерную колбу вместимостью 50 мл, растворяют в 45 мл спирта этилового 70 %, доводят спиртом 70% до метки и перемешивают. 5 мл полученного раствора помещают в мерную колбу вместимостью 25 мл, доводят спиртом 70%, подкисленным серной кислотой до метки и перемешивают.
Измеряют оптическую плотность испытуемого раствора при длине волны 465 нм, в кювете с толщиной слоя 10 мм. В качестве раствора сравнения используют спиртом 70%, подкисленный серной кислотой. Параллельно измеряют оптическую плотность и раствора СО сангвиритрина.
Содержание суммы алкалоидов в пересчете на сангвиритрин в ЛРС в % (Х, %) вычисляют по формуле:
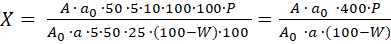 , где
, где
А0 – оптическая плотность раствора СО сангвиритрина;
А – оптическая плотность испытуемого раствора;
a0 – навеска СО сангвиритрина, г;
a – навеска сырья, г;
W- потеря в массе при высушивании, %;
Р – содержание основного вещества в СО сангвиритрина, %.
Приготовление подкисленного спирта 70%: к 6 частям (по объему) спирта 70% прибавляют 1 часть 1% раствора серой кислоты и перемешивают. Срок годности раствора 7 сут.
Приготовление 1% раствора серной кислоты: к 1 л воды прибавляют 6,1 мл концентрированной серной кислоты и перемешивают. Срок годности раствора 1 мес.
Результаты и обсуждение
Бензо[с]фенантридиновые алкалоиды имеют выраженное поглощение в УФ-области, при этом вклад в суммарное поглощение вносят все остальные изохинолиновые алкалоиды и другие вещества, содержащиеся в ЛРС маклейи. Спектр поглощения в УФ-области спектра суммы алкалоидов и сангвиритрина в этиловом спирте приведен на рис.1.
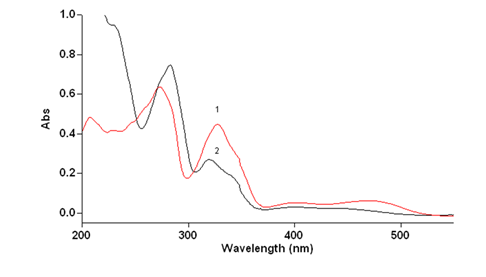
Рисунок 1.Спектр поглощения раствора СО сангвиритрина (1) и извлечения из травы маклейи (2) в спирте 70%, подкисленном серной кислотой
Для минимизации систематической и случайной погрешности определения в методике использован стандартный образец - сангвиритрин.
Близкие по структуре и свойствам четвертичные бензофенантридиновые алкалоиды сангвинарин и хелеритрин в форме оснований бесцветны, но образуют ярко-окрашенные соли. Сангвинарин с азотной или серной кислотами образует соли оранжево-красного цвета, хелеритрин - желтого.
Выраженная интенсивность поглощения сангвиритрина в спирте 70%, подкисленном серной кислотой, в УФ-области, в максимумах при 273 и 327 позволяют использовать это свойство для оценки содержания всей суммы алкалоидов в пересчете на сангвиритрин, как в виде солей, так и оснований, но определить сумму только сангвинарина и хелеритрина не представляется возможным, т.к. значения оптической плотности и результаты будут сильно завышены.
Определение суммы сангвинарина и хелеритрина целесообразно проводить по поглощению в диапазоне 350-500 нм, по максимумам поглощения их окрашенных солей. Эта особенность позволяет отделить их от других неокрашенных солей изохинолиновых алкалоидов маклейи, например, протопина и алокриптопина, которые также содержатся в сырье и вносят значительные вклад в поглощение в УФ-области.
В качестве растворителя для приготовления испытуемого раствора используют спирт 70%, подкисленный серной кислотой, рабочая концентрация раствора сангвиритрина составила 0,004 % (0,04 мг/мл). Спектр сангвиритрина в диапазоне длин волн от 350 до 550 нм характеризуется максимумами при длине волны 402 и 465 нм, последний целесообразно использовать в качестве аналитического, т.к. таковой при 402 нм может давать завышенные результаты за счет вклада сопутствующих компонентов.
Извлечения из травы маклейи имеет максимум при длине волны 402±2 и максимум или плечо при 465±2 нм. Поэтому измерение целесообразно проводить в видимой части спектра, при длине волны 465 нм, специфичной для сульфатов сангвинарина и хелеритрина (рис.2)
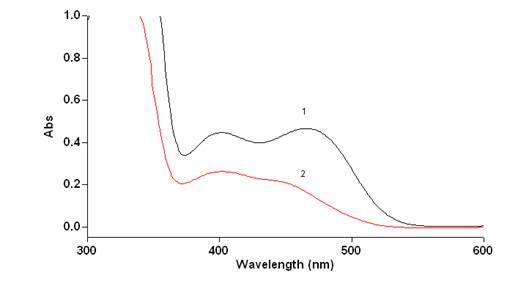
Рисунок 2. Спектр поглощения раствора СО сангвиритрина (1) и извлечения из травы маклейи (сумма алкалоидов) в спирте 70%, подкисленном серной кислотой (2)
Разработка методики с использованием метода спектрофотометрии при анализе бензо[с]фенантридиновых алкалоидов для получения точных и воспроизводимых результатов нуждается в таких условиях, при которых на интенсивность поглощения в аналитическом максимуме не оказывали сопутствующие вещества, соизвлекаемые с анализируемыми алкалоидами. В связи с этим, важным этапом разработки методики стал подбор условий экстракции, которые позволили бы исключить токсичные растворители, сократить время определения, а также оптимизировать точность и воспроизводимость. Использование органических растворителей может обусловить получение завышенных результатов из-за вклада соизвлекаемых окрашенных веществ в поглощение, например, каратиноидов, хлорофиллов и глубоко окрашенных димерных пигментов [34].
Хлороформ с водой и водно-спиртовыми растворами в щелочной среде создает стойкие эмульсии, что значительно уменьшает точность количественного определения алкалоидов, увеличивая время, сложность, использование дополнительного оборудования (центрифуги). На извлечение алкалоидов оказывает влияние температура, при настаивании с хлороформом при комнатной температуре в течение 30 мин нельзя достичь исчерпывающей экстракции, это обстоятельство очень сильно влияет на погрешность определения. Поэтому в методике ФС 42-2666-89 время настаивания длительно и составляет 15 ч.
Поскольку изохинолиновые алкалоиды успешно извлекаются этанолом, то в качестве экстрагента использован 70% этиловый спирт. Экстракцию проводили при соотношении сырье – экстрагент 1:50 при нагревании на кипящей водяной бане. Полученное извлечение подщелачивали аммиаком и основания алкалоидов экстрагировали этилацетатом. Для избавления от сопутствующих веществ проводили реэкстракцию подкисленной водой и вторую экстракцию этилацетатом. Последовательная реэкстракция оказывает значительнее влияние на результаты, по экспериментальным оценкам оптической плотности, сопутствующие алкалоидам окрашенные вещества, поглощающие в аналитической области, могут увеличивать оптическую плотность на 20-30% от поглощения собственно суммы алкалоидов.
В качестве аналитической выбрана длина волны 465 нм. Анализ сырья, поступающего в ВИЛАР, показал, что содержание суммы сангвинарина и хелеритрина (бисульфатов) варьирует в значительных пределах (от 0,08 % до 1,35 %), что в значительной степени согласуется с результатами анализов некоторых образцов травы маклеи по методике ФС 42-2666-89 (содержание суммы алкалоидов в пересчете на сангвиритрин составило 0,07 - 1,04%). Такое сырье с относительно невысоким содержанием суммы алкалоидов пригодно для переработки, поэтому целесообразно изменить норму содержания алкалоидов на соответствующую реальным показателям, т.е. не менее 0,08%.
В соответствии с требованиями ГФ ХV для разработанной аналитической методики определены валидационные характеристики. Определение линейности проводилось на 10 уровнях концентраций СО сангвиритрина в диапазоне 8,5 – 77 мкг/мл (Рис. 3), линейная зависимость имеет вид y=0,0111x-0,0622
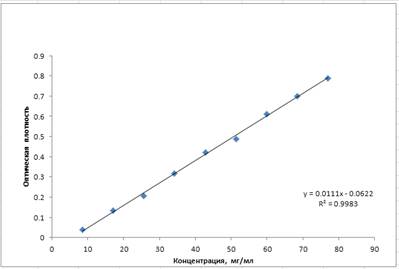
Рисунок 3. График зависимости оптической плотности от концентрации сангвиритрина
Зависимость оптической плотности от концентрации СО сангвиритрина прямо пропорциональна в диапазоне концентраций 8,5 – 77 мкг/мл, коэффициент корреляции близок к единице (0,9983), что служит критерием для подтверждения линейности.
Испытания по определению правильности методики количественного определения суммы сангвинарина и хелеритрина (бисульфатов) в пересчете на сангвиритрин в траве маклейи проводили на извлечении из ЛРС с добавлением известного количества СО сангвиритрина. Модельные смеси готовили трех концентраций с содержанием СО сангвиритрина 25, 50, 75 % к исходной концентрации в сырье маклейи (Табл. 1).
Таблица 1. Результаты испытания по определению правильности методики количественного определения суммы сангвинарина и хелеритрина (бисульфатов) в пересчете на сангвиритрин в траве маклейи сердцевидной
|
№ п/п |
Найдено, мг |
Добавлено СО, мг |
Заданное значение, мг |
Полученное значение, мг |
Абсолютная ошибка |
Выход, % |
|
1.1 |
0,2886 |
0,0512 |
0.3398 |
0.3388 |
-0.0010 |
99.71 |
|
1.2 |
0,2886 |
0,0512 |
0.3398 |
0.3365 |
-0.0033 |
99.03 |
|
1.3 |
0,2886 |
0,0512 |
0.3398 |
0.3351 |
-0.0047 |
98.62 |
|
2.1 |
0,2886 |
0,1024 |
0.3910 |
0.3916 |
+0.0006 |
100.15 |
|
2.2 |
0,2886 |
0,1024 |
0.3910 |
0.3911 |
0.0001 |
100.03 |
|
2.3 |
0,2886 |
0,1024 |
0.3910 |
0.3896 |
-0.0014 |
99.64 |
|
3.1 |
0,2886 |
0,1536 |
0.4422 |
0.4408 |
-0.0014 |
99.68 |
|
3.2 |
0,2886 |
0,1536 |
0.4422 |
0.4412 |
-0.0010 |
99.77 |
|
3.3 |
0,2886 |
0,1536 |
0.4422 |
0.4421 |
-0.0008 |
99.98 |
|
Среднее значение процента восстановления, % |
99,62 |
|||||
В разработанной методике процент восстановления находился в пределах от 99,79% до 100,33% и имеет среднее значение 99,62%, что соответствует требованиям критерия приемлемости. Сходимость (прецизионность) разработанной методики устанавливали на двух различных образцах ЛРС в пяти повторностях в одной и той же лаборатории одним и тем же аналитиком с использованием одного и того же оборудования и реактивов, в пределах одного рабочего дня (Табл. 2).
Таблица 2. Результаты испытания по определению сходимости методики количественного определения суммы сангвинарина и хелеритрина (бисульфатов) в пересчете на сангвиритрин в траве маклейи сердцевидной и маклейи мелкоплодной
|
Повторность |
Содержание суммы солей сангвинарина и хелеритрина в пересчете на сангвиритрин в траве маклейи, % |
|
|
Маклейя сердцевидная |
Маклейя мелкоплодная |
|
|
1 |
0.294 |
0.188 |
|
2 |
0.285 |
0.186 |
|
3 |
0.291 |
0.181 |
|
4 |
0.293 |
0.188 |
|
5 |
0.289 |
0.184 |
|
Среднее значение |
0,290 |
0.185 |
|
Стандартное отклонение (SD) |
0.0036 |
0,0030 |
|
Относительное стандартное отклонение (RSD), % |
1.23 |
1,60 |
Относительное стандартное отклонение составило 1,23 и 1,60%, что свидетельствует о прецизионности методики в условиях повторяемости.
Внутрилабораторная воспроизводимость методики подтверждалась на одном и том же образце ЛРС маклейи в трех повторностях на разных спектрофотометрах. Полученные результаты приведены в Табл. 3.
Таблица 3. Результаты испытания по определению воспроизводимости методики количественного определения суммы суммы сангвинарина и хелеритрина (бисульфатов) в пересчете на сангвиритрин в траве маклейи сердцевидной
|
Прибор |
Повторности |
Содержание суммы солей сангвинарина и хелеритрина в пересчете на сангвиритрин в траве маклейи, % |
|
1 |
1 |
0,294 |
|
2 |
0.285 |
|
|
3 |
0.291 |
|
|
2 |
1 |
0.281 |
|
2 |
0.289 |
|
|
3 |
0.286 |
|
|
Среднее значение содержания суммы алкалоидов в анализируемом растворе, % |
0.288
|
|
|
Стандартное отклонение (SD) |
0,0046 |
|
|
Относительное стандартное отклонение (RSD), % |
1,61 |
|
Коэффициент вариации составил 0,73%, что позволяет считать внутрилабораторную воспроизводимость результатов приемлемой.
Выводы. Разработанная методика определения суммы солей сангвинарина и хелеритрина в пересчете на сангвиритрин в траве Macleaya cordata и Macleaya microcarpa, по сравнению с фармакопейной, имеет ряд преимуществ - позволяет сократить длительность анализа с более чем 15 ч до 2 ч; исключает расход токсичных растворителей (хлороформа, дихлорэтана и метанола).
Методика валидирована, экспериментально подтверждена ее специфичность (совпадение максимумов поглощения при длине волны 465±2 нм); линейность (коэффициент корреляции 0,998); правильность (процент восстановления находится в пределах от 99,79% до 100,33%, среднее значение 99,62%), относительная погрешность среднего результата разработанной методик не превышает ±3,5 %.
Сравнение содержания суммы алкалоидов в образцах ЛРС разных видов маклейи показало, что содержание суммы солей сангвинарина и хелеритрина в пересчете на сангвиритрин в Macleaya cordata выше более чем в полтора раза, чем в Macleaya microcarpa.
Conflict of interest
Библиографическая ссылка
Копытько Я.Ф. РАЗРАБОТКА ЭКСПРЕССНОЙ МЕТОДИКИ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ СУММЫ САНГВИНАРИНА И ХЕЛЕРИТРИНА (БИСУЛЬФАТОВ) В ПЕРЕСЧЕТЕ НА САНГВИРИТРИН В ТРАВЕ МАКЛЕЙИ МЕТОДОМ СПЕКТРОФОТОМЕТРИИ // Научное обозрение. Химические науки. 2025. № 1. ;URL: https://science-chemistry.ru/en/article/view?id=64 (дата обращения: 25.05.2026).
 science-review.ru
science-review.ru